 2024年的第一个月,FDA先后对SMOK、suorin、BLU PLUS、Bidi stick电子烟品牌的部分产品下发营销拒绝令(MDO),这意味着这些公司不得在美国营销或分销这些产品,否则将面临 FDA 执法行动的风险。FDA上一次下发MDO还是在2023年10月,时隔两个月后密集地下发MDO,在全美最大TPE展会展开前,FDA的举动意味着什么?这会是美国对电子烟的新一轮监管的开始吗?
2024年的第一个月,FDA先后对SMOK、suorin、BLU PLUS、Bidi stick电子烟品牌的部分产品下发营销拒绝令(MDO),这意味着这些公司不得在美国营销或分销这些产品,否则将面临 FDA 执法行动的风险。FDA上一次下发MDO还是在2023年10月,时隔两个月后密集地下发MDO,在全美最大TPE展会展开前,FDA的举动意味着什么?这会是美国对电子烟的新一轮监管的开始吗?
【两个至上原创】美国食品药品监督管理局(FDA)对雾化电子烟的监管在2024年似乎再次收紧,但部分中国厂商还在等待属于自己的“船票”。
2024年的第一个月,FDA先后对SMOK、Suorin、BLU PLUS、Bidi stick电子烟品牌的部分产品下发营销拒绝令(MDO),这意味着这些公司不得在美国营销或分销这些产品,否则将面临 FDA 执法行动的风险。FDA上一次下发MDO还是在2023年10月,时隔两个月后密集地下发MDO,在全美最大TPE展会展开前,FDA的举动意味着什么?这会是美国对电子烟的新一轮监管的开始吗?
 FDA在2024年下发的四次MDO|图源:FDA
FDA在2024年下发的四次MDO|图源:FDA
四个品牌,分属三品类
两个至上对1月以来FDA下发的MDO的产品进行了盘点,发现四个品牌的产品涉及到了开放式电子烟、换弹式电子烟、一次性电子烟等三品类,而其中既有中国公司、也有英国公司。FDA的动作似乎有意将雾化电子烟的所有品类在2024年开年做一次“点名”。且这些产品在各自的类型中都有足够的知名度,并不是无人知晓的小品牌、小厂家。
1月16日,SMOK的22款电子烟产品被FDA下发营销拒绝令(MDO),被拒绝的产品包括烟具设备、烟仓、雾化器和烟弹。两个至上统计后发现,SMOK这次“被拒”的22个产品分属六个系列,皆为开放式电子烟产品,以下为具体分类列表:
SMOK OSUB ONE 系列:
- SMOK OSUB ONE Device
- SMOK OSUB ONE RPM Cartridge
- SMOK OSUB ONE RPM Cartridge 3 Pack
SMOK RPM 系列:
- SMOK RPM DC 0.8 Ω MTL ATOMIZER
- SMOK RPM DC 0.8 Ω MTL ATOMizer 5 Pack
- SMOK RPM 40 Device
- SMOK RPM Empty Standard Cartridge
- SMOK RPM Empty Nord Cartridge
- SMOK RPM Mesh 0.4 Ω Atomizer
- SMOK PRM 2 Mesh 0.16 Ω Atomizer
- SMOK RPM Mesh 0.4 Ω Atomizer
SMOK Nfix 系列:
- SMOK Nfix Device
- Nfix DC 0.8 Ω MTL Pod
SMOK POZZ 系列:
- SMOK POZZ Device
- SMOK POZZ DC 0.8 Ω Pod
SMOK Nord 系列:
- SMOK Nord DC 0.8 Ω MTL Atomizer
- SMOK Nord 2 Device
- SMOK Nord 2 RPM Cartridge
- SMOK Nord 2 Nord Cartridge
SMOK SCAR-P3 系列:
- SMOK SCAR-P3 Device
- SMOK SCAR-P3 Empty RPM 2 Cartridge
- SMOK SCAR-P3 Empty RPM Cartridge
 SMOK OSUB ONE套装|图源:SMOK
SMOK OSUB ONE套装|图源:SMOK
仅在三天之后的1月19日,FDA又向深圳市你我网络科技有限公司(Shenzhen YouMe InforMATion Technology Co. Ltd)的两款Suorin电子烟产品和帝国烟草子公司 Fontem US, LLC 的 blu PLUS+ 的多款电子烟产品发出了拒绝销售令(MDO)。
其中Suorin电子烟产品为Suorin Air与Suorin Air empty refillable cartridge,分别为烟具与空烟弹产品,从产品介绍看,Suorin Air是一款可注油换弹式产品;而blu PLUS+则是一款“可充电的一次性电子烟”。
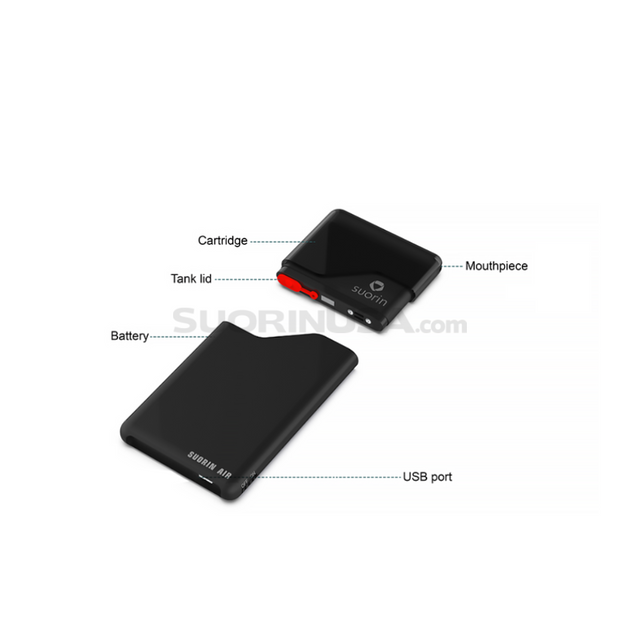 Suorin Air|图源:Suorin
Suorin Air|图源:Suorin  blu PLUS+® Carolina Bold 2.0% |图源:blu
blu PLUS+® Carolina Bold 2.0% |图源:blu
但FDA的的行动并未结束,又3天后的1月22日,FDA向Bidi Vapor LLC的Bidi Stick Classic电子烟下发MDO,据官网介绍Bidi Stick Classic为一款一次性产品。
 Bidi Stick Classic|图源:Bidi Stick
Bidi Stick Classic|图源:Bidi Stick
主动求合规的公司们
FDA对新型烟草的审核缓慢一直为人诟病,截至2023年3月,通过PMTA的电子烟产品不过23种。仍有大量的电子烟产品还未从FDA获得初步的结果。
FDA为PMTA设计了一套复杂但是具有针对性的审查,所有提交公司的产品都必须满足这些审核,两个至上查阅FDA官网的流程介绍,以下为精简步骤:
提交前会议:申请人与FDA之间的自愿正式会议,讨论烟草制品计划中的PMTA提交;
验收审查:行政审查,以确保产品归入烟草制品中心管辖,确认满足申请的法律和法规要求;
提交审查:确定申请是否包含足够信息以允许进行实质性审查的阈值;
实质审查:FDA对申请中的科学信息和数据的评估,输出量缺陷证明:需要其他信息才能做出营销授权决定。申请人有180天的时间回复此类信函;
审查结果:发布营销令或拒绝营销令。
上市后报告:要求申请人建立和维护FDA必要的记录,并作出报告,以确定或促进确定是否有理由撤回或暂时中止市场批准的订单。
 审核环节|图源:FDA
审核环节|图源:FDA
例如2024年第一个被下发MDO的SMOK,其官网资料显示:
2020年7月,向FDA提交其电子尼古丁输送系统产品的预上市烟草产品申请(PMTA)
2020年8月,SMOK收到美国食品药物管理局的烟草产品上市前申请受理函;
2020年9月,SMOK 通过第二轮烟草产品上市前申请并进入最后阶段。
 SMOK提交PMTA的声明|图源:两个至上
SMOK提交PMTA的声明|图源:两个至上
在提交PMTA的当时,SMOK在美国市场的占有率仍保持较高水平,据FDA联合美国疾病预防与控制中心(CDC)发布的2021年全国青少年烟草调查数据显示,9.6%的青少年表示他们使用SMOK产品,而JUUL位居其后,比例为5.7%。
 全国青少年烟草调查,美国,2021 年|图源:CDC
全国青少年烟草调查,美国,2021 年|图源:CDC
在提交PMTA申请的的三年半后,1月16日,SMOK最终等来了“被拒”的消息,但SMOK品牌的所属公司深圳市艾维普思科技有限公司(IVPS)已宣布已向美国第五巡回上诉法院提起上诉,反对美国食品药品监督管理局(FDA)对其SMOK品牌开放式电子烟套装及相关备件的营销拒绝令。
 SMOK称会起诉FDA|图源:SMOK
SMOK称会起诉FDA|图源:SMOK
据公开资料显示,SMOK也是2020年9月9日前提交PMTA的6家中国电子烟企业之一,值得注意的是,你我集团旗下Suorin也在其中,在本月同样被下发了MDO。
同一批的还有思摩尔旗下自有大烟品牌VAPORESSO、电子烟供应链合元集团、吉迩旗下大烟品牌VOOPOO、以及Boulder。
本次同样被FDA下发MDO的Suorin,其在2020年8月20日的IECIE 2020中,公布了PMTA申请流程, Suorin称在当年的5月之前提交的申请材料,且对“内容和质量充满信心”。Suorin表示,已提交PMTA申请包括HPHC测试、可提取物和可浸出物测试、稳定性研究、毒理学分析、临床试验和感知研究的结果和总结。
 Suorin在IECIE 2020的讲解|图源:IECIE 2020
Suorin在IECIE 2020的讲解|图源:IECIE 2020
除了这两家明确被拒绝的企业外,还有四家电子烟厂商的PMTA悬而未决,等待着FDA的答复,也就是审查结果公布阶段。两个至上在查阅相关资料后,对2024年1月25日前,它们的申请状态作出如下梳理。
美国时间2020年8月27日正式提交PMTA并通过首轮审核;
2020年9月5日通过第一轮审核;
2020年9月30日通过第二轮审核。
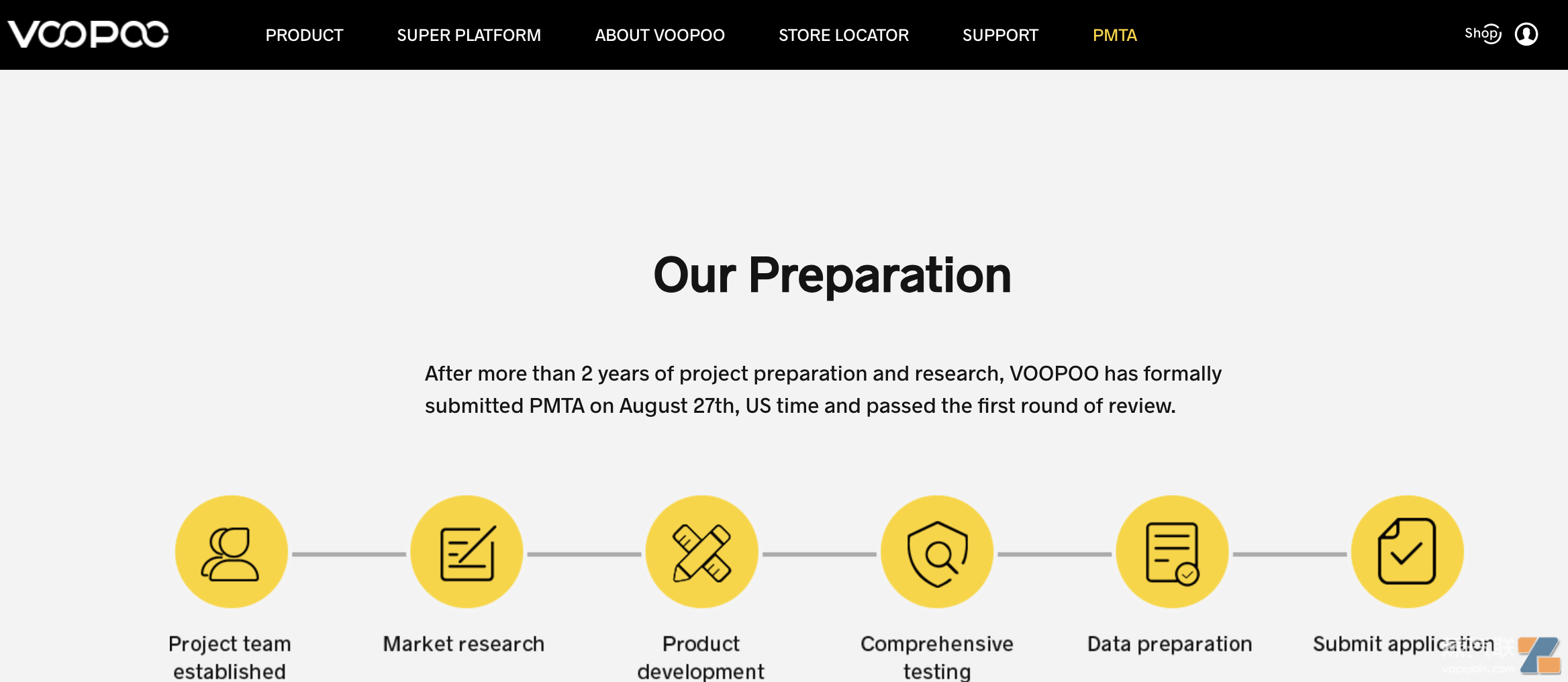 VOOPOO官网对PMTA进度的介绍|图源:VOOPOO
VOOPOO官网对PMTA进度的介绍|图源:VOOPOO
据VOOPOO的介绍,其“整个项目进程斥资亿元 ,从准备到申请历时20个月,完成了产品成分分析、制造研究、非临床及临床人体研究等PMTA检测要求。”
目前VOOPOO的申请仍在FDA的审核状态。
Boulder是唯一同时提交烟油与设备的中国厂商,其于2020年9月8日向FDA提交了六款烟油和三款设备的PMTA。据悉,这是第一家在美国提交电子烟油PMTA的中国电子烟公司。并已通过第二轮审核,进入实质性科学审查阶段。Boulder在2022年01月21日发布的一份稿件提到,“铂德是唯一一家进入PMTA实质性科学审查阶段的中资企业。”
从2020年10月3日,Vaporvoice的报道情况看,Boulder将初始申请仅包含四种设备,分别是两种设备:Boulder Rock 和 Aspen Slim,以及两种口味的电子烟油:American Blend 和 Menthol。
 Boulder对PMTA进度的介绍|图源:Boulder
Boulder对PMTA进度的介绍|图源:Boulder
与VOOPOO类似,Boulder的申请还未得到FDA的最终回应。
作为中国电子烟供应链企业,思摩尔国际和合元集团的PMTA申请与合作企业关联性更强。
据美国FDA的规定,客户和代工厂需要共同向FDA递交PMTA认证,如代工企业配合客户进行PMTA申请时,需要提供样品和文档,并且工厂也需要通过检验。而客户如果需要更换代工方,则其产品需要重新通过PMTA申请。基于以上原因,产品一旦通过认证不会轻易更换代工厂。
国内供应链巨头之一的合元集团宣布,于2020年8月25日接到FDA受理函。该通知将 firstunion 提交的材料移至 PMTA 程序的实质性审查阶段;2020年9月8日,合元集团完成PMTA申请第二轮审核,并收到FDA的备案函。
 合元集团收到PMTA 备案函|图源:VAPTIO
合元集团收到PMTA 备案函|图源:VAPTIO
合元集团曾表示,在进入实质性审查阶段之前,经过一年多的努力,完成了超过10万页的申请材料和支持其主张的证据,以及多维度的测试数据和报告来证明公司的产品有利于公众健康。
据两个至上了解,合元集团是唯二的一家已经被FDA现场审核过的中国电子烟工厂,另一家则是思摩尔。
思摩尔作为代工企业,其代工的产品有多款已获得PMTA,据思摩尔发布的2023年中报告,“FDA已为本集团为客户生产的11款封闭式系统的烟草味ENDS产品发布了上市许可”。同时,思摩尔国际也为自己的开放式电子烟品牌VAPORESSO申请PMTA。
2020 年 8 月 20 日,VAPORESSO 首轮 PMTA 申请获 FDA 受理;
2020 年 9 月 1 日,VAPORESSO提交的首批PMTA产品已通过FDA第二轮备案阶段;
2021年3月12日,Vaporesso 对 FDA 缺陷函做出回应;
2021年4月8日,Vaporesso已完成FDA远程监管评估。
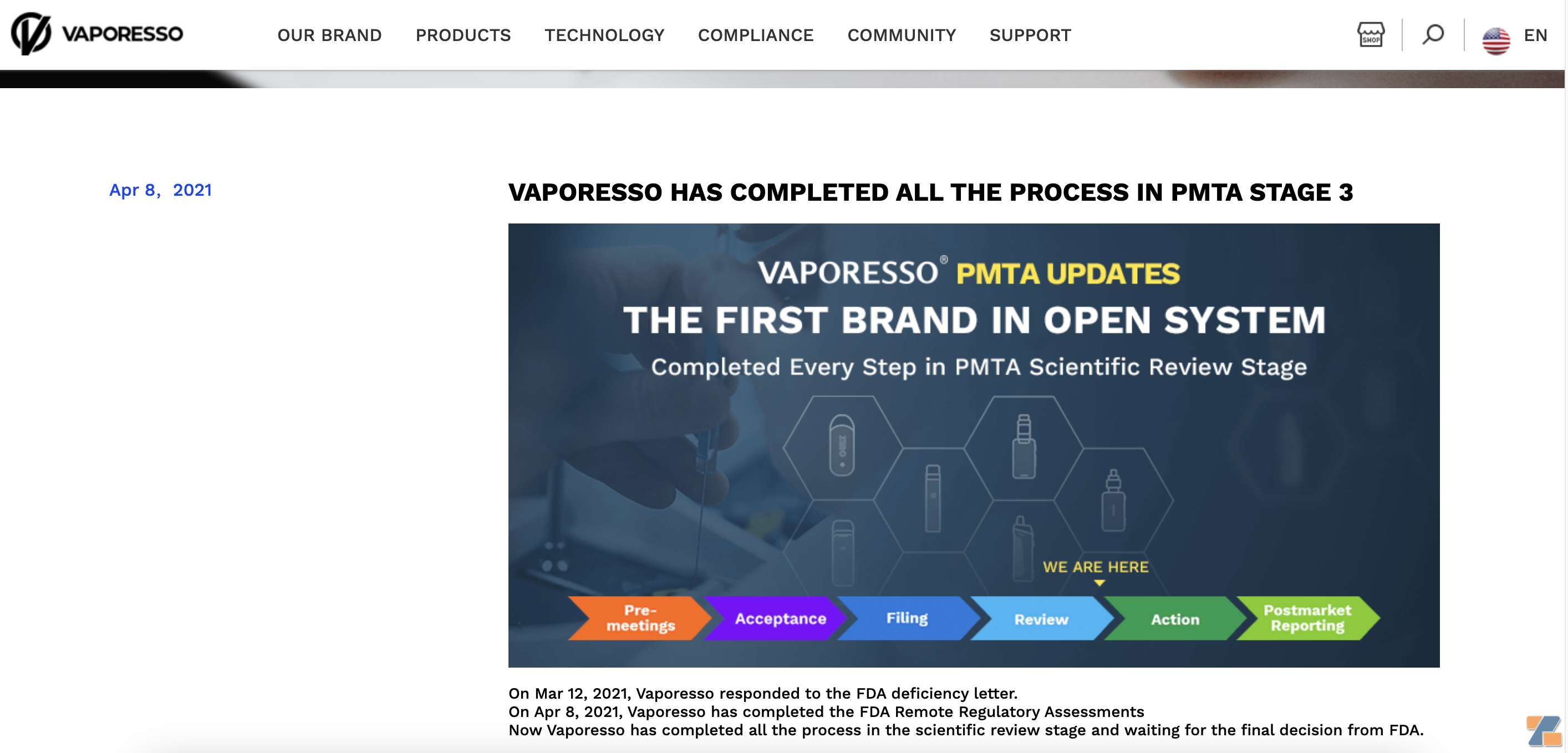 Vaporesso度PMTA的介绍|图源:Vaporesso
Vaporesso度PMTA的介绍|图源:Vaporesso
Vaporesso官网介绍显示,其已完成科学审查阶段的所有流程,正在等待FDA的最终决定。
回顾2020年出海潮
以上企业仅盘点了2020年9月9日前提交PMTA的6家中国电子烟企业,国内企业会想奔赴美国获得PMTA,实则是国内外形势的变化。
2019年11月1日,国家烟草专卖局、国家市场监督管理总局联合发布《关于进一步保护未成年人免受电子烟侵害的通告》(以下简称“通告”):敦促电商平台及时关闭电子烟店铺,并将电子烟产品及时下架;敦促电子烟生产、销售企业或个人及时关闭电子烟互联网销售网站或客户端;敦促电子烟生产、销售企业或个人撤回通过互联网发布的电子烟广告。
 国家烟草专卖局、国家市场监督管理总局联合发布《关于进一步保护未成年人免受电子烟侵害的通告》|图源:
烟草局网站
国家烟草专卖局、国家市场监督管理总局联合发布《关于进一步保护未成年人免受电子烟侵害的通告》|图源:
烟草局网站
中国电子烟的网络监管从此有法可依,但是此时已经有不少的企业锚定出海,遥望大洋彼岸的美国,电子烟行业最具潜力的新星JUUL正在逐渐走向衰落,中国发布《通告》的前一个月,2019年10月18日,JUUL宣布在美国停售调味电子烟,只保留烟草和薄荷类口味。一个超级“独角兽”的暂时性地退场留给市场其他企业创造了机会。
 JUUL宣布在美国停售调味电子烟|图源:CBS
JUUL宣布在美国停售调味电子烟|图源:CBS
次年1月,FDA颁布了美国电子烟新政,禁止调味电子烟烟弹,仅保留烟草和薄荷醇两种口味。被向全球第一大电子烟市场美国进军。而PMTA作为合法销售的必要凭证,似乎成了出海前的船票。
 FDA颁布了美国电子烟新政,禁止调味电子烟烟弹|图源:FDA
FDA颁布了美国电子烟新政,禁止调味电子烟烟弹|图源:FDA
2020年,中国的电子烟企业还在寻求如何获得PMTA,当时行业预计“PMTA的严苛标准,也将让电子烟海外市场迎来新一轮洗牌”。但很少有人注意到一次性电子烟在全球的兴起,这类使用门槛极低、抽吸便捷、可以随时丢弃的电子烟,在短短几年内征服了美国乃至全球各地的消费者。
2023年的美国全国青少年烟草调查结果显示,当前电子烟用户中最常报告使用的品牌是:ELFBAR(56.7%)、Esco Bars(21.6%)、Vuse(20.7%)、JUUL(16.5%)和Mr. Fog(13.6%)。
前文提到,电子烟品牌JUUL在巅峰期2018年,市场占有率曾达76%,而最新的尼尔森便利店数据显示,Juul的市场份额从24.3%下降到24.2%,位列市场第二,第一名则是英美烟草的VUSE。
 电子烟品牌JUUL在巅峰时期的占有率曾达76%|图源:ncbi
电子烟品牌JUUL在巅峰时期的占有率曾达76%|图源:ncbi
但VUSE和JUUL都不是真正的“优胜者”,尼尔森的报告主要涵盖了大型连锁店,因此,雷诺烟草和奥驰亚估计,这些非法产品占据美国电子烟市场大约一半的份额。
这其中绝大多数就是一次性产品,根据分析公司Circana持有的行业数据,目前在美国商店销售的电子烟产品超过11,500种,较6月的9,000种增长了27%。
FDA目前仅对23款电子烟发放了营销许可,这意味着市场99%的雾化电子烟都属于官方法律下的非法产品。FDA在2023年更是停止新的雾化电子烟产品的通过,2023年全年,这一数字维持在0。
2021年10月12日,Vuse Replacement Cartridge Original 4.8% G2成为有史以来第一款通过PMTA申请的雾化电子烟,2022年6月10日,NJOY DAILY Rich Tobacco 4.5%通过了PMTA,成为截止2024年1月为止的最后一款获得MGO(营销许可令)的雾化电子烟产品。
 FDA目前仅对23款电子烟发放了营销许可|图源:FDA
FDA目前仅对23款电子烟发放了营销许可|图源:FDA
但前者属于被英美烟草收购的雷诺烟草旗下品牌,后者则在2023年3月6日被奥驰亚宣布收购,NJOY 共有6款产品获得FDA的PMTA许可。。
中国厂商目前还没有一款电子烟产品通过PMTA审核被下发MGO,讽刺的是,中国电子烟产品占据着美国市场绝大部分的份额,但“有名无实”,而申请PMTA的企业们,它们的期盼的合法身份,仍悬而未决。









